
AI創薬支援
プラットフォーム
Drug Discovery AI Factory
創薬の仮説生成
AI「KIBIT」、
「自然言語」、
「創薬研究者」
が創薬の起点となる
「仮説」を生み出す
Drug Discovery AI Factoryの特長
新規性
自社開発AI「KIBIT」を活用し、疾患関連性の高い未報告の標的分子を発見
高確度
独自の解析手法で成功確度の高い標的分子を抽出
仮説生成
遺伝子ネットワークを作成し、未報告の標的分子に関する仮説を生成
KIBITを活用し、未報告の標的遺伝子を多数抽出
独自の解析手法を用いてさらに確度の高い標的に絞り込みます
KIBITは、非連続的発見という新しいアプローチによって、“未報告”、つまり論文に記載されていない関連性を発見する、自社開発の自然言語処理AIエンジンです。Drug Discovery AI Factoryでは、KIBITを活用し、疾患に関連する遺伝子・分子のつながりを解析したネットワークを構築します。その際、疾患との関連性が未報告の標的分子をも予測します。このネットワークをベースに、革新的な解析手法「Drug Discovery Best Known Method(DD-BKM)」を活用し、新薬の成功確度の高い標的分子に絞り込みます。
例:疾患Aの遺伝子ネットワーク
:疾患Aとの関連性が高く、その関連性が論文に記載されていない標的分子
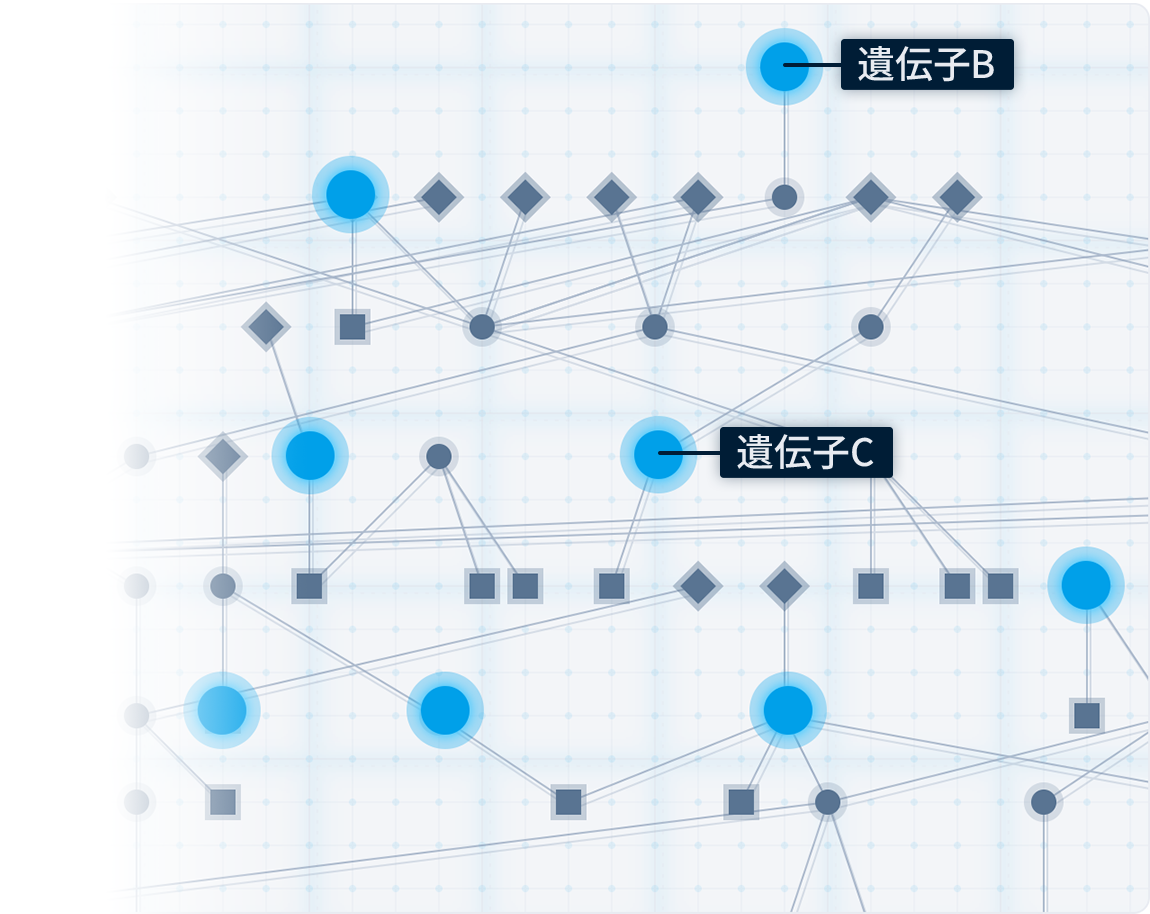
遺伝子B・遺伝子Cともに
疾患Aとの関連は報告されていない
創薬成功確度の高い遺伝子を抽出
:疾患Aとの関連性が高く、その関連性が論文に記載されていない標的分子から成功確度の高い標的分子を抽出

解析例
KIBITによる仮想的な実験
(Virtual Experiments)
注目する遺伝子を仮想的にノックアウト(KO)し、パスウェイがどのように変化するかをシミュレーションします。
例えば下図では、遺伝子Bを仮想的にKOしても、遺伝子Dに置換されるだけでネットワークへの影響はほぼない一方で、遺伝子Cをノックアウトした場合にはネットワークが大きく変化し、遺伝子Cが疾患に影響を及ぼす遺伝子であることが推測されます。
既知情報から未報告の関連性を発見する独自技術
論文上では疾患との関連性が記載のない遺伝子・分子まで予測します
解析対象の論文データはPubMedが中心で、Springer Natureの論文データをオプションで加えることができます。
FRONTEOの創薬支援サービスは、論文情報から新規性の高い標的分子を抽出してくるところに特徴があります。
既知の論文情報をKIBITが読み取り未報告の関連性を導き出す
Springer Nature
拡張機能
フルテキスト解析・アブストラクト解析の比較
KIBITの解析対象となる遺伝子数が増加することで、
より新規性の高い標的分子を発見することができます
アブストラクトで報告されるまでのタイムラグを埋め、
平均5年早く標的分子を発見することを可能にします
創薬研究に長年従事してきた専門家が顧客のニーズに合った提案を実現
KIBITは、非連続的発見という新しいアプローチによって、“未報告”、つまり論文に記載されていない関連性を発見する、自社開発の自然言語処理AIエンジンです。Drug Discovery AI Factoryでは、KIBITを活用し、疾患に関連する遺伝子・分子のつながりを解析したネットワークを構築します。その際、疾患との関連性が未報告の標的分子をも予測します。このネットワークをベースに、革新的な解析手法「Drug Discovery Best Known Method(DD-BKM)」を活用し、新薬の成功確度の高い標的分子に絞り込みます。
FRONTEOの考える仮説
新薬の開発を始めるための仮説は、
- 標的分子:疾患との関連が予測される遺伝子・分子など
- 疾患メカニズム:標的分子がどのように疾患に関連するかなど
- 患者情報:対象と考える患者群ゲノム情報や疾患、症状など
- 安全性情報:候補となる薬剤の毒性など
- フィジビリティ:実験モデル提案など
創薬研究で新しいアイデアや方向性を生み出すための仮説を生成し、持続的に供給します。
Contents
コンテンツ
- HOME >
- AI創薬支援プラットフォーム



