
仮説生成に特化した発見型概念検索AIシステム「KIBIT Amanogawa」
2023.12.19
疾患ゲノム解析と自然言語処理AI「KIBIT」の融合による新規創薬標的探索の実現
2024.02.07
医薬品創出難度の高まった昨今、製薬企業にとって既存製品のLCMや諸般の事情により開発を断念した社内休眠化合物の活用、すなわちDrug Repositioning(DR:ドラッグリポジショニング)は喫緊の課題の一つです。DRにおいて、膨大な医学・薬学情報の網羅的かつ客観的な解析は新規性の高い適応症候補を見出す上で必須です。しかし、通常、このプロセスを短期間で効率的に進めることは困難と言わざるを得ません。
ここでは、網羅性、客観性および圧倒的スピードで、ヒトでは気付き難い新規適応症候補の発見を可能とする、FRONTEO独自の自然言語処理AIエンジン「KIBIT」をベースとしたDRソリューションに関して、Target X (GPCR)の解析事例と共に紹介します。

Speaker
株式会社FRONTEO
ライフサイエンスAI事業本部
ライフサイエンスAI研究チーム 担当部長
博士(薬学)
林 一己
薬学博士号を取得後、山之内製薬(現アステラス製薬)に入社。炎症・循環器・腎臓領域を担当しリサーチマネージャーとして活躍。ドラッグリパーパシング室を立ち上げDR研究に従事。KIBITを用いた解析方法の考案、解析方針立案、解析、仮説生成を担当。
Drug Repositioning
Drug Repositioning(DR:ドラッグリポジショニング)
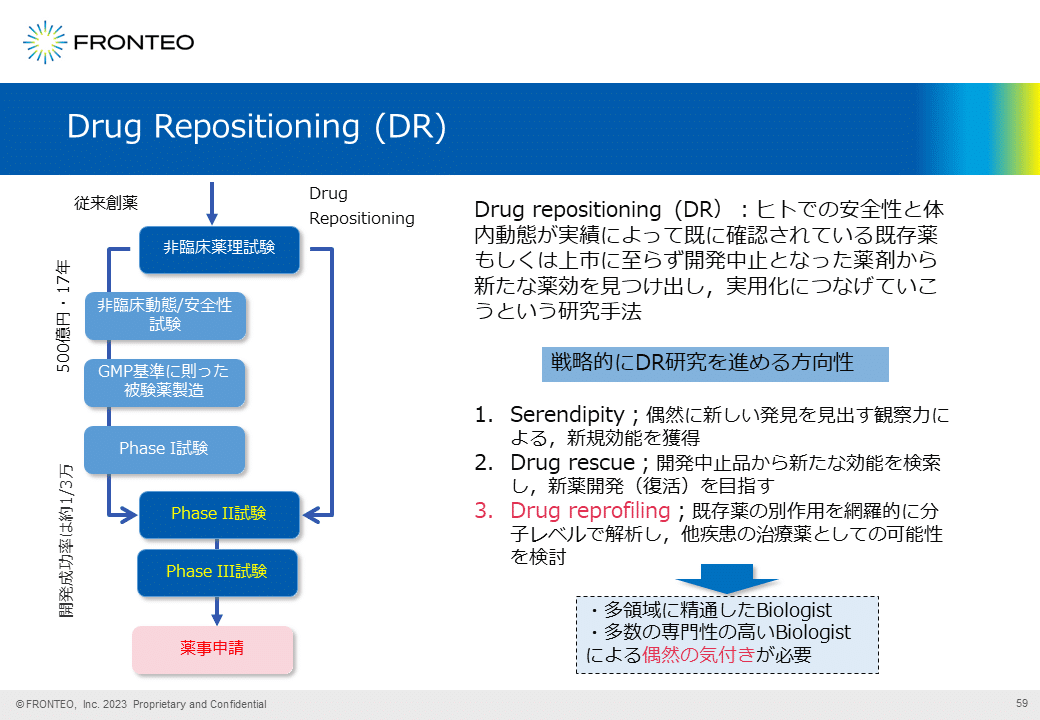
従来型の創薬は、多額のコストをかけて長期に渡って研究しても、成功確度は3万分の1程度と試算されています。
しかし、Drug Repositioning(ドラッグリポジショニング)なら、すでに化合物なども存在していますので、まず非臨床の薬理試験(POC in animal)にて動物における候補物質の効果が認められれば、その後の数ステップをスキップし、フェーズⅡから開始して承認を得るという取り組みを進めることも可能です。
ドラッグリポジショニングは昔から考えられてはいましたが、研究者のセレンディピティに依存するところが大きいのが実情で、ドラッグレスキューやドラッグリプロファイリング(いずれもスライド画像参照)で戦略性を持たせる努力はされているものの、最後は研究者の偶然の気づき(セレンディピティ)に頼っています。
この部分を必然的に気づかせることができるのが、FRONTEOの「多面的解析」です。
過去のドラッグリポジショニング成功事例
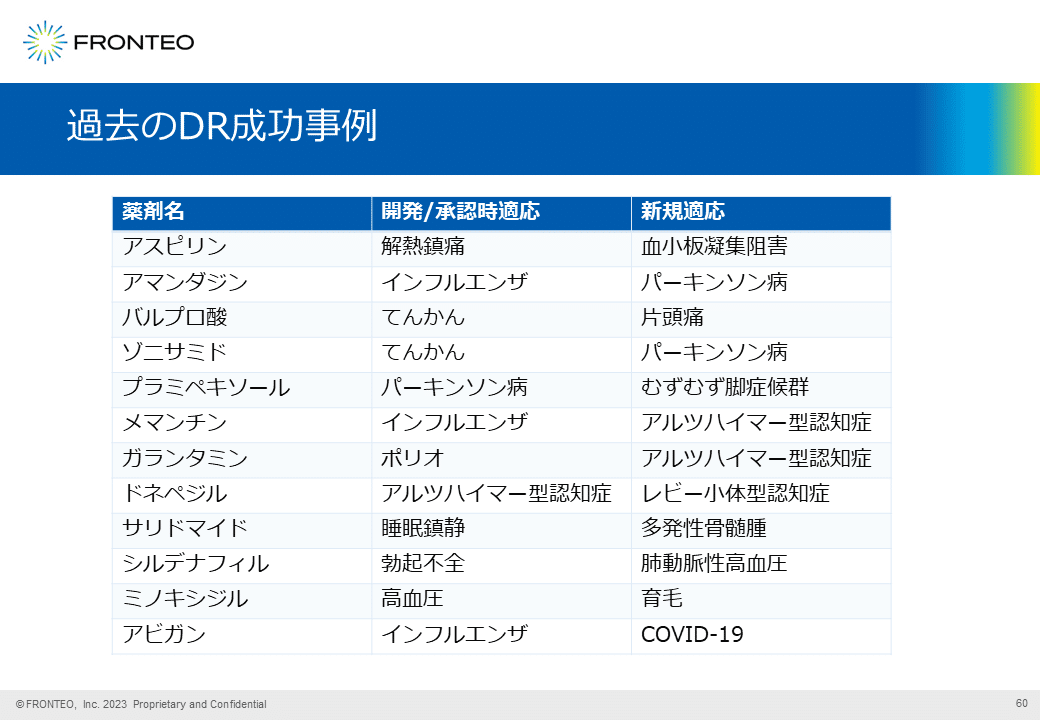
ドラッグリポジショニングの過去の成功事例を振り返ると、てんかんから片頭痛またはパーキンソン病など、似て非なるものとはいえ同じような臓器のため思いつきやすいものもあれば、インフルエンザからアルツハイマー型認知症のように、感染症から中枢性の疾患などへとかなりジャンプしたドラッグリポジショニング事例も存在します。
この気づきを、FRONTEOの多面的解析を用いて皆さまに達成していただきたいと思っています。
ドラッグリポジショニング対象疾患候補策定方法
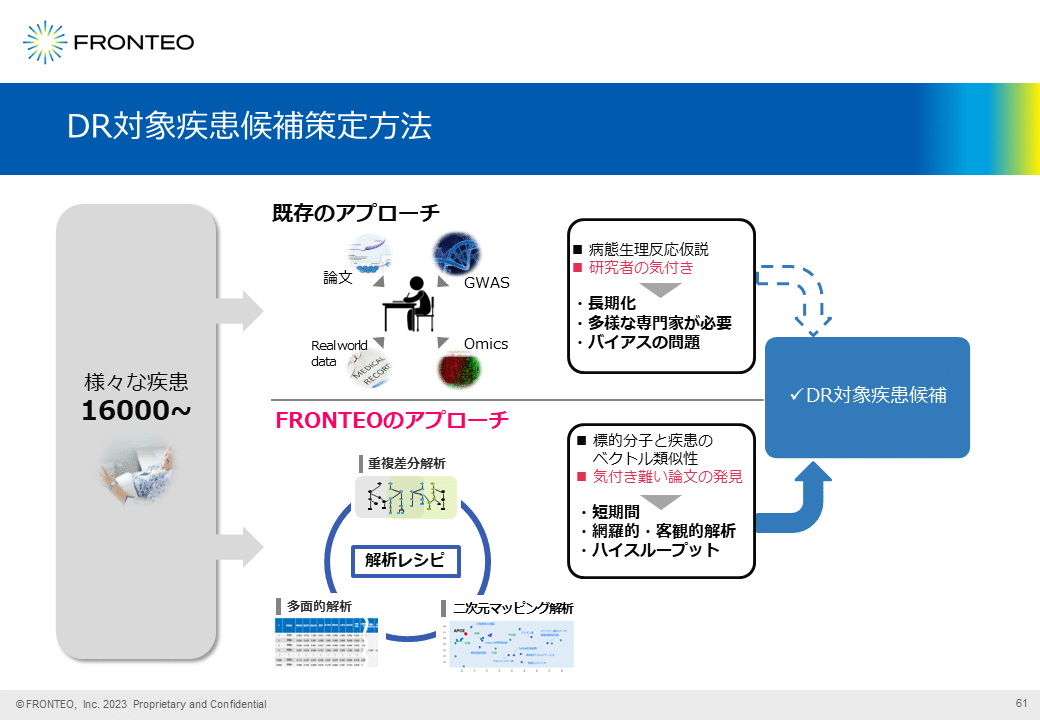
ドラッグリポジショニングでは、研究者が様々な情報を活用しながら1万6000以上の疾患を対象に疾患候補を策定し、仮説を生成します。ここで問題になるのは研究者自身のバイアスと多様性です。興味のあるまたは専門性のある疾患領域や生物学分野に偏ってしまい、限定的な疾患しか挙げられない可能性があります。情報量も非常に多いことから、長い時間を費やさなければ新たな疾患候補は見出せません。
FRONTEOの解析レシピを利用すれば、網羅的で客観的な解析を行うハイスループット手法により、短期間で対象疾患を策定することができます。人の目では気づきにくい論文も発見できるため、想定を超えた新しい適応症に対する気付きを得ることも可能です。
Drug Discovery Best Known Methods
Drug Discovery Best Known Methods
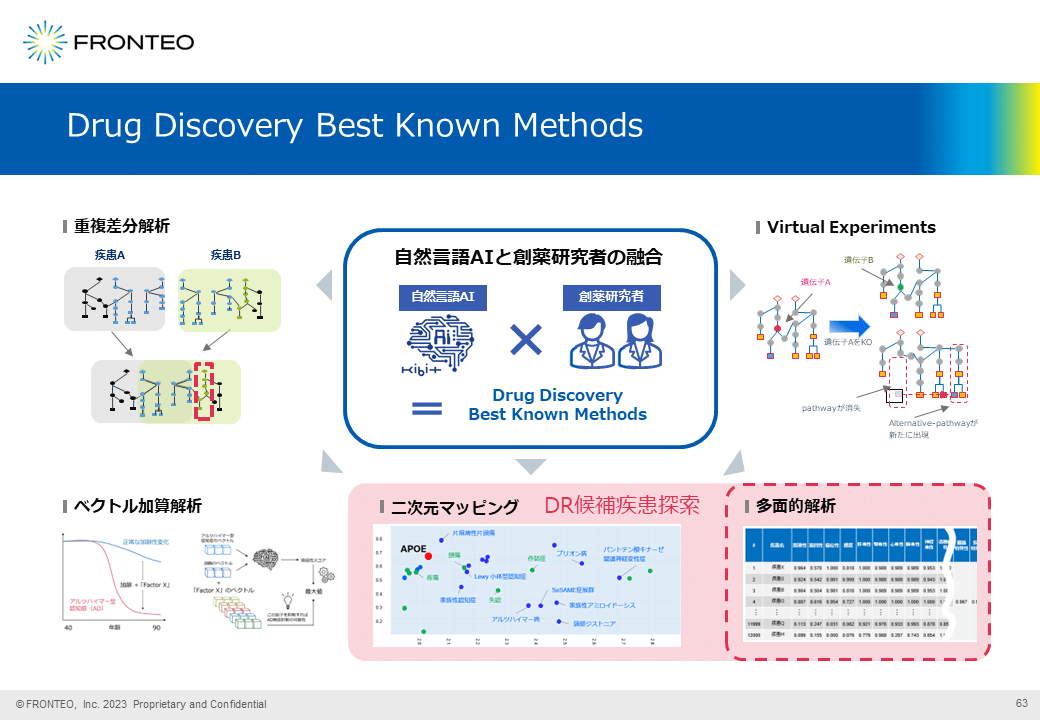
FRONTEOでは5つの解析手法「Drug Discovery Best Known Methods」を持っています。自社開発の自然言語処理AI 「KIBIT」をベースに解析し、AIから得られた解析結果を創薬研究の実務経験者がさらに解釈し、創薬につながる仮説を生成します。
ドラッグリポジショニングの疾患探索では、このうち「二次元マッピング」または「多面的解析」を活用します。今回は「多面的解析」の活用例を紹介します。
多面的解析:KIBIT liGALILEOとは
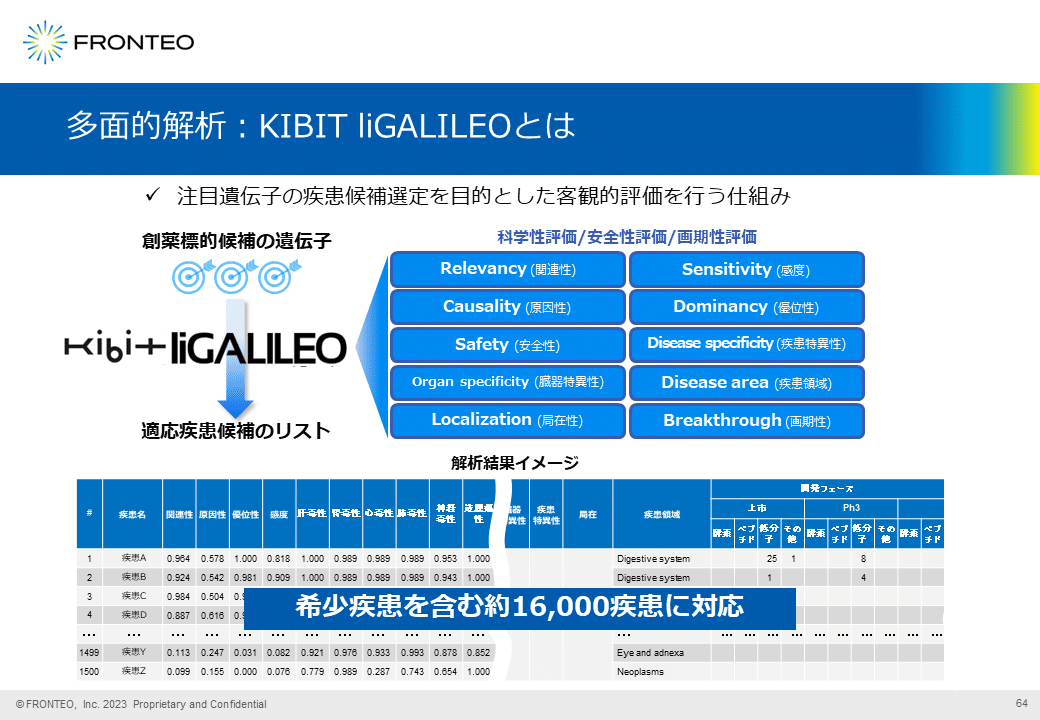
多面的解析とは、注目する遺伝子の疾患候補選定を目的とした客観的評価を行うシステムです。
基本評価項目は10種類です。まず科学性評価項目である関連性・原因性・優位性・感度の4つのスコアの平均値で、疾患がランク付けされます。
残る6つの安全性や画期性などの情報を活用して、製薬会社様の戦略に則った疾患を選定することが可能なシステムです。このシステムで、希少疾患を含む約1万6000の疾患を対象に解析できます。
多面的解析:科学性評価項目スコアの見方
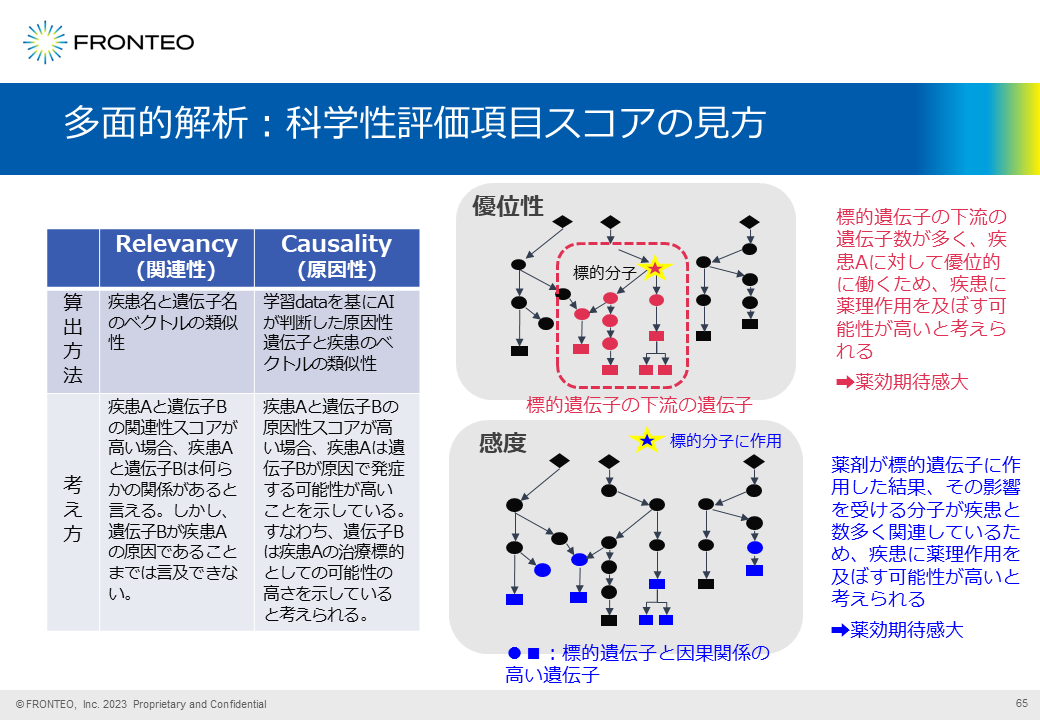
科学性評価項目について簡単に説明いたします。
「関連性」は、疾患名と遺伝子名のベクトルの類似性をスコア化したもの、「原因性」は、学習データを元にAIが判断した原因性遺伝子と疾患のベクトルの類似性をスコア化したものです。
「優位性」と「感度」は、どちらも薬効期待感を示す項目です。
「優位性」は、FRONTEOオリジナルの疾患ネットワーク(遺伝子名にて構成される)に注目する標的遺伝子が存在した場合、その下流に連なる遺伝子数を元にスコアを算出します。つまり、その標的遺伝子の影響を受けやすい遺伝子が多く存在すれば、この標的遺伝子に対して低分子化合物等のモダリティを作用させた場合、疾患に対する薬理作用が発現しやすいだろう、という考え方で算出するスコアです。
「感度」は、優位性と同様の疾患ネットワークに注目する標的遺伝子が存在しなくとも、標的遺伝子と因果関係が高い遺伝子がそのネットワークに多く存在するならば、標的遺伝子に対して低分子化合物等のモダリティを作用させた場合、疾患に薬理作用を及ぼす可能性が高いだろう、という考え方で算出するスコアです。
ドラッグリポジショニング対象疾患候補策定事例
排他性を担保する疾患の絞り込み
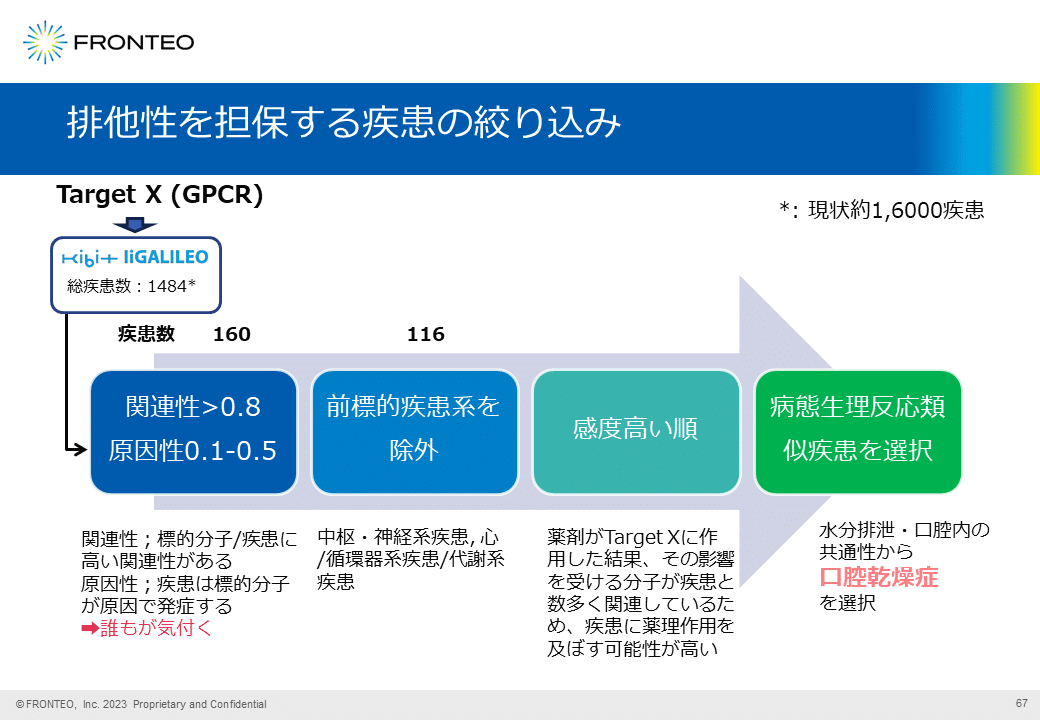
続いて、事例について紹介します。この解析は2年半ほど前に実際に行ったもので、当時の対象疾患は1500程度でしたが、それを現在は1万6000まで増やしています。
今回の例はGPCRであるTarget Xを対象に、多面的解析でドラッグリポジショニング対象疾患の策定を実施しました。解析後に疾患候補が1位から約1500位まで並ぶ中からの疾患選定は非常に難しいことから、今回はドラッグリポジショニングする上で課題となる「対象化合物の物質特許の残存期間も短い」という点を解決する「排他性を担保できそうな疾患を選択する戦略」で、疾患候補の絞り込みを行いました。
まず、疾患と標的遺伝子との関連性が高いことは必須なため、関連性のスコアは高く(>0.8)し、原因性のスコアが高い疾患は誰もが気づく疾患であることから原因性のスコアは低め(0.1~0.5)に設定し、絞り込みを行いました。その結果、10分の1程度の160疾患まで絞り込むことができました(4段階の一番左)。
さらに前テーマ(過去の研究時)の標的疾患をすべて除外すると、116疾患になりました(左から2番目)。ここまで絞り込めば、人の目で確認することも可能になってきますので、次に薬効期待感の高い順、つまり感度の高い順に並び替え、上から順番に見ていきました。
病態の類似性をヒントに、口腔乾燥症を選択し、深掘り調査を行って仮説を生成します。この絞り込みステップを、これから実例で紹介します。
フィルタリング前の上位29位
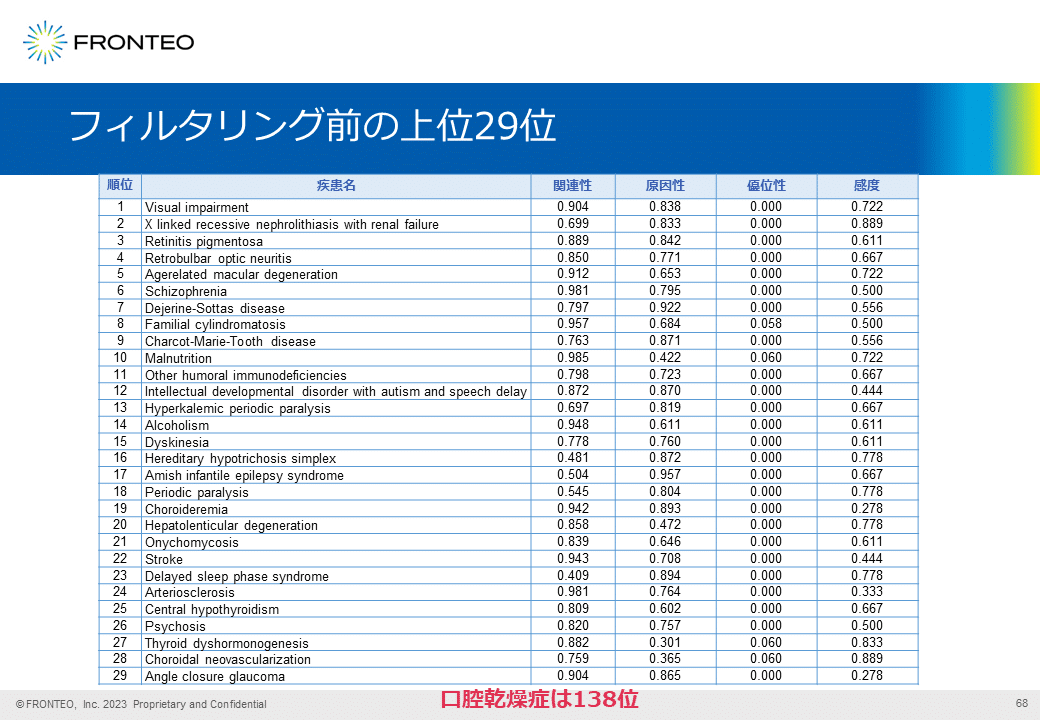
多面的解析を行った直後は1484疾患まで並ぶうち、上位30疾患程度の元データは画像のとおりで、「口腔乾燥症」は138位でした。
関連性と原因性のスコアで絞り込み
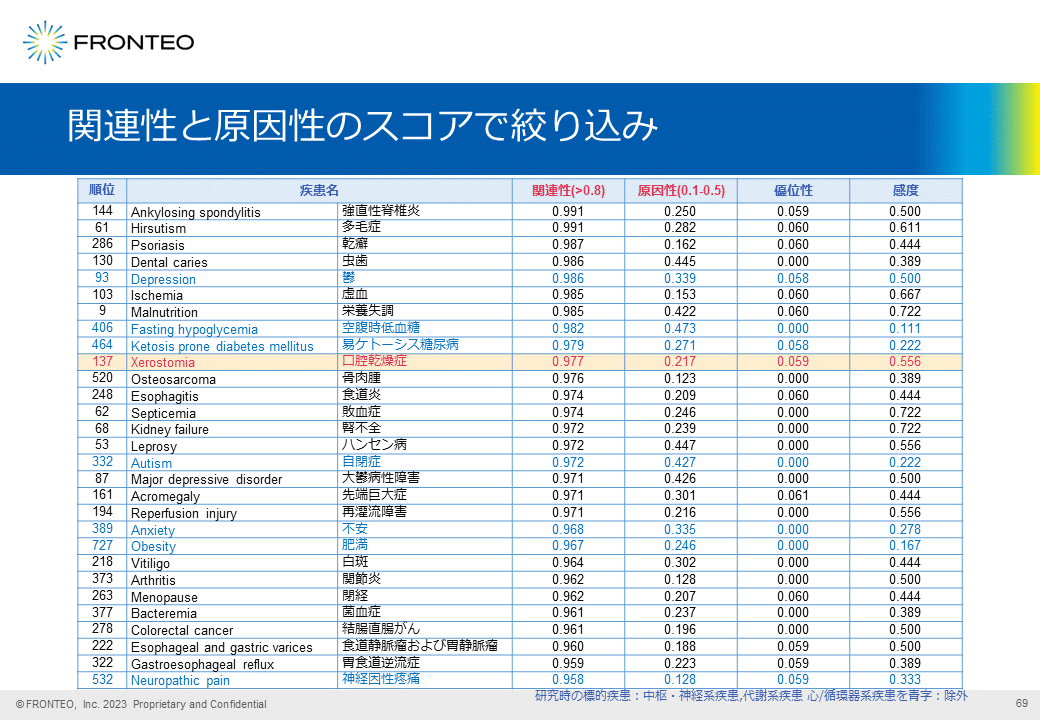
関連性と原因性のスコアで絞り込むと「口腔乾燥症」は10位にランキングします。また、青字で示している前テーマ(過去の研究時)の標的疾患を削除していきます。
感度のスコアで絞り込み
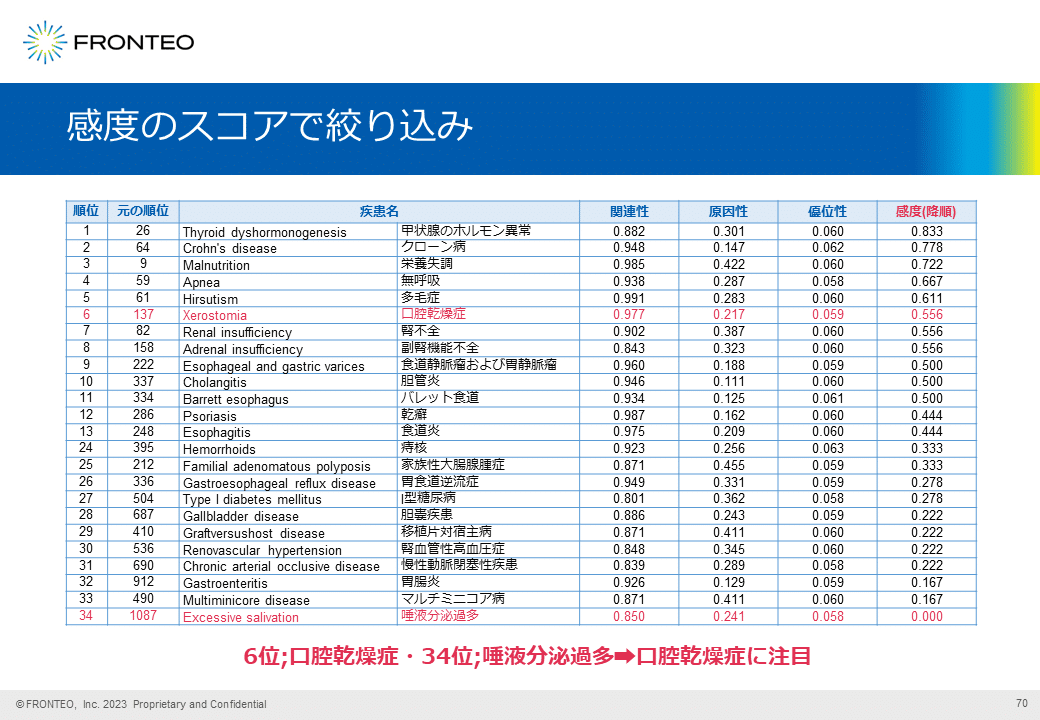
最後に、感度の高い順に並び変えると、「口腔乾燥症」は6位にランキングします。そして34位に真逆の唾液分泌過多がランキングされたので、この類似性を元に唾液分泌に注目しました。
以上から、最終的にランキングが高く感度のスコアが存在する「口腔乾燥症」を選択して調査を継続しました。
口腔乾燥症(Xerostomia, Dry Mouth)
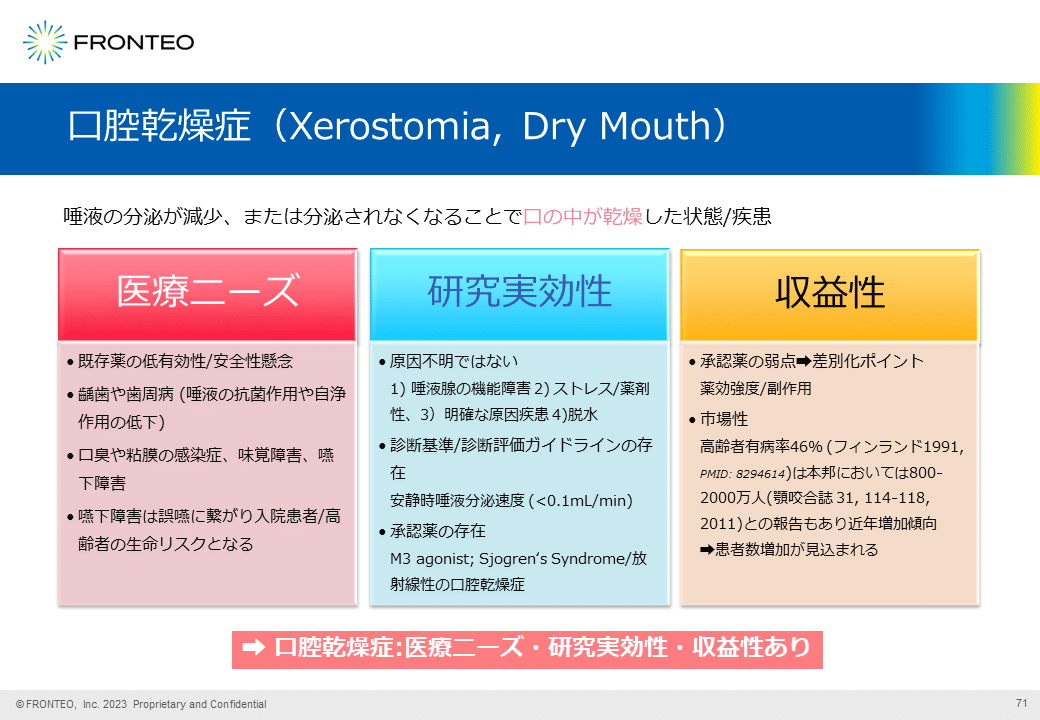
実際に創薬研究を行う上では、この口腔乾燥症が本当に「疾患」であること、あるいは「医療ニーズ」や「研究の実効性」・「収益性」があるかという要素も重要であることから、簡易的な調査にて確認後、仮説生成を実施していきます。
なお、疾患か否かについては、口腔乾燥症は口腔内が乾燥した状態であり、「疾患」であると定義づけられています。
・医療ニーズ
既存薬の有効性が低いこと、安全性の懸念が高いことから、新たな薬剤が求められているのではないかと考えられます。また口腔乾燥症は、嚥下障害が誤嚥(ごえん)の原因であることから、高齢者にとって口腔乾燥症は生命のリスクとなると考えられます。つまり口腔乾燥症には医療ニーズがあると考えられます。
・研究実効性
ガイドラインかつ承認薬も存在する事から、研究は実行可能であると考えられます。
・収益性
差別化ポイントは、医療ニーズにも挙げた薬効強度と副作用面ではないかと考えられます。超高齢化社会を迎えつつある世情を鑑みると、高齢者の口腔乾燥症は増加すると予想されるため、市場性もあると考えられます。
これらの要素が満たされたので、創薬研究する意義が存在する「疾患」と考え、詳細調査を行って仮説生成を実施しました。
唾液分泌促進作用:M3作動薬 vs 物質A(Target X 刺激物質)
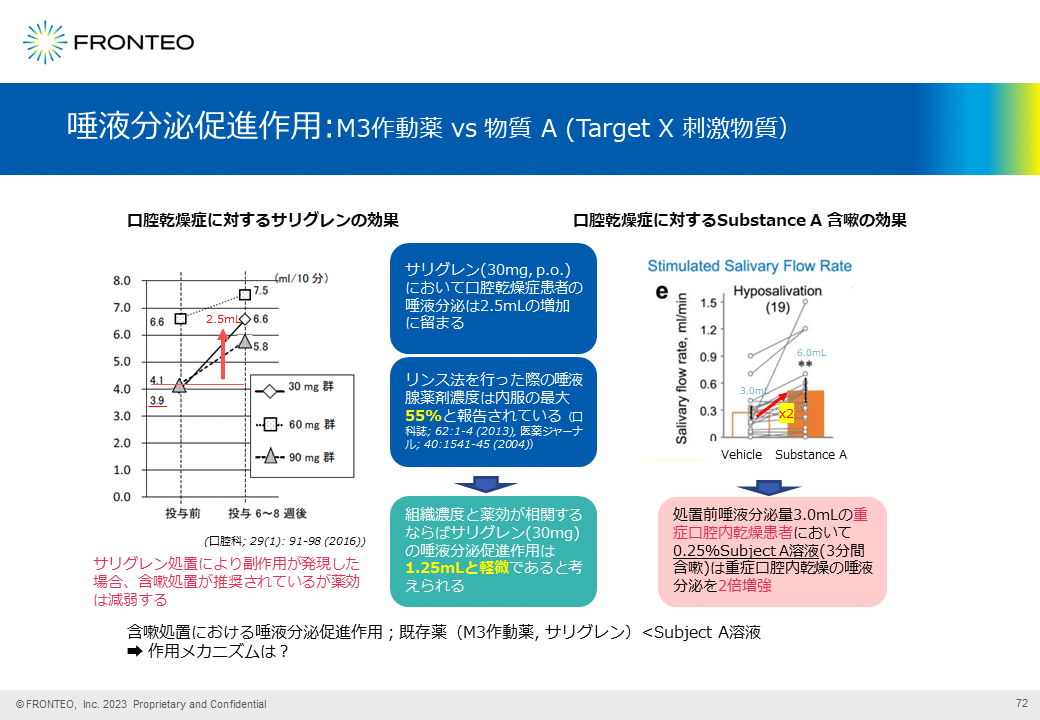
口腔乾燥症の標準薬であるM3作動薬と、今回のTarget Xの刺激物質の臨床効果の報告をご紹介します。
唾液分泌量が通常(10mL)から約4割に低下した口腔乾燥症の患者さんに対し、M3作動薬であるサリグレンを30mg経口投与すると2.5 mLほどの唾液分泌の亢進作用が確認されています。
しかし、サリグレンの内服は副作用が問題となり、しばしば口腔内リンスとして使用されます。リンス法を行った場合の唾液腺組織内の薬剤濃度は、内服時の50%程度であると報告されています。組織内濃度と薬効が相関すると仮定すると、サリグレン30mgを内服ではなく口腔内リンスで用いた場合、唾液分泌の亢進は1mL程度の軽微な効果しか期待できないという計算になります。
一方、Target Xの刺激物質を含嗽(がんそう)処置した場合は、サリグレンの効果を検討した患者さんより少し重症な患者さん(3 mL程度の唾液分泌)に対し3mLの唾液の亢進作用が報告されています。
以上の結果から、既存薬であるM3作動薬に比べ、Target Xの刺激剤は強力な唾液分泌促進作用を示す可能性が示唆されます。安全性においては、同標的に対するアゴニスト活性を有する別化合物の臨床試験(別疾患)情報から、サリグレンに比べて副作用面において大きな問題がないと考えられます。
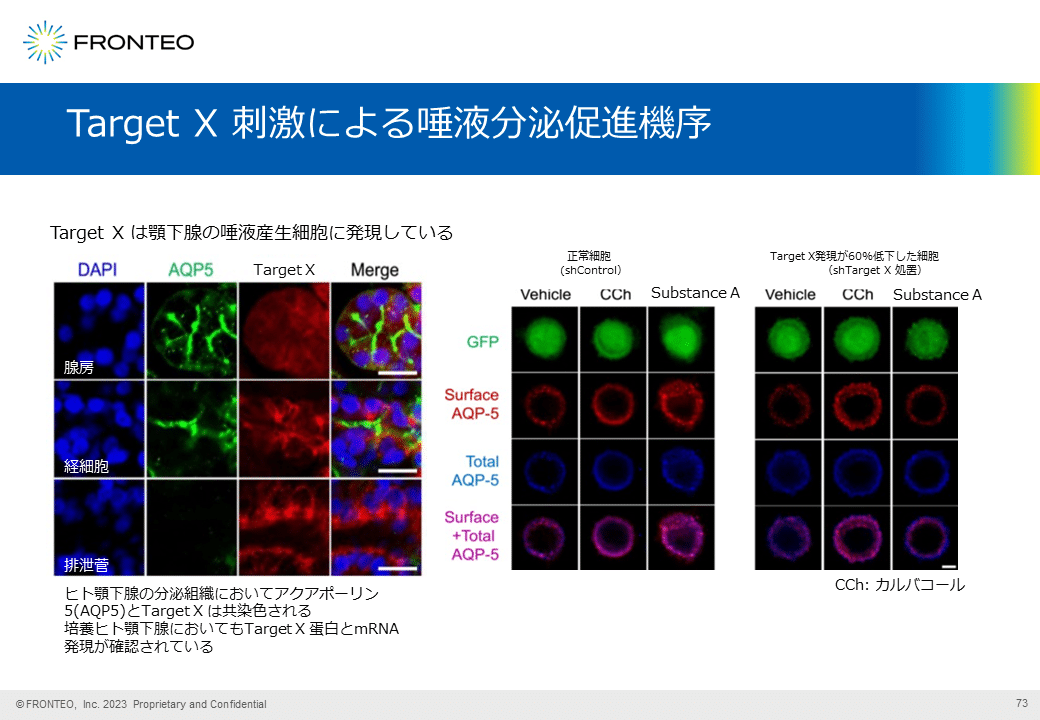
Target X 刺激における唾液分泌促進機序
作用メカニズムについて次に紹介していきます。
まずTarget Xの唾液分泌組織への発現についてご紹介します。唾液腺房細胞または唾液腺経細胞には、唾液分泌をつかさどるアクアポーリン5(AQP5)とTarget Xが共発現している事が報告されていることから、Target Xは標的組織に発現していると考えられます。
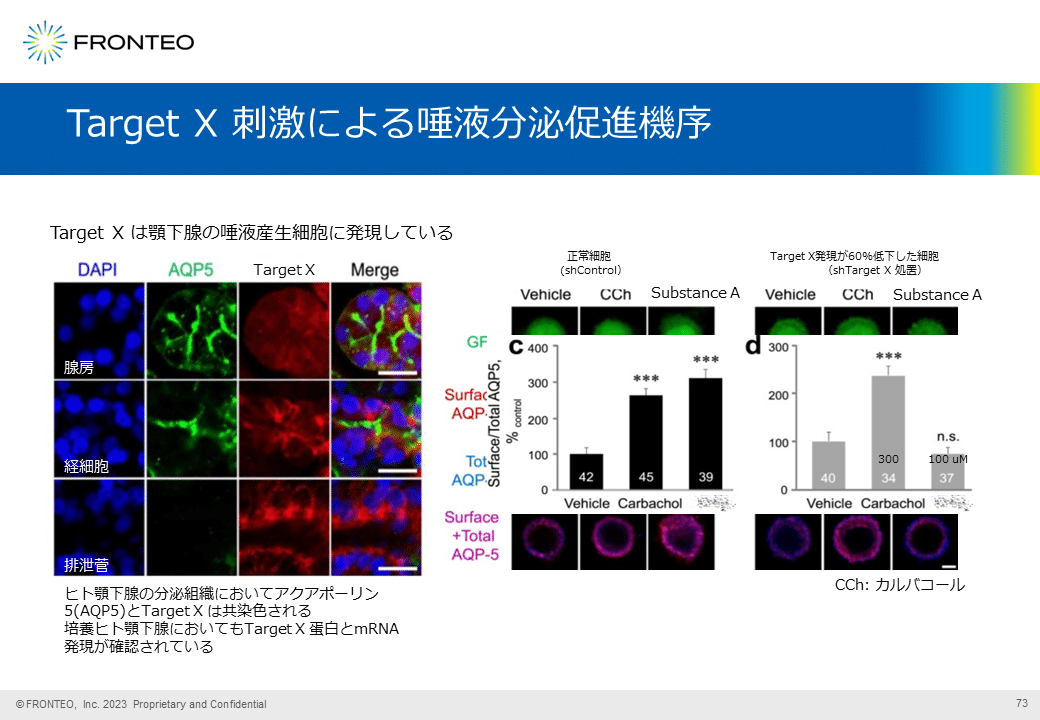
実際の作用メカニズムは、健常人の唾液腺細胞を用いたin vitro 実験で検証されています。方法はTarget Xのノックダウン実験です。
shRNAはどの細胞にもほぼ均一に導入されています(最上段FITC)。コントロールのshRNAを導入した場合は、ムスカリン作動薬であるカルバコールまたはTarget Xの刺激物質によって、細胞膜上のAQP5発現が亢進します(2段目)。
しかし、Target X shRNAにてTarget Xをノックダウンした場合、Target Xの刺激による細胞膜上のAQP5発現亢進作用は消失しますが、M3刺激作用には変化がありません。

以上より、Target Xの作用機序は唾液腺細胞膜におけるAQP5の発現亢進である可能性が示唆されます。
さらに調査を進めると、Target Xを刺激した場合に唾液腺細胞の増殖が起こることが報告されていることから、M3作動薬では期待できない寛解も狙えると考えられます。
Target Xと口腔乾燥症の関連の予見性
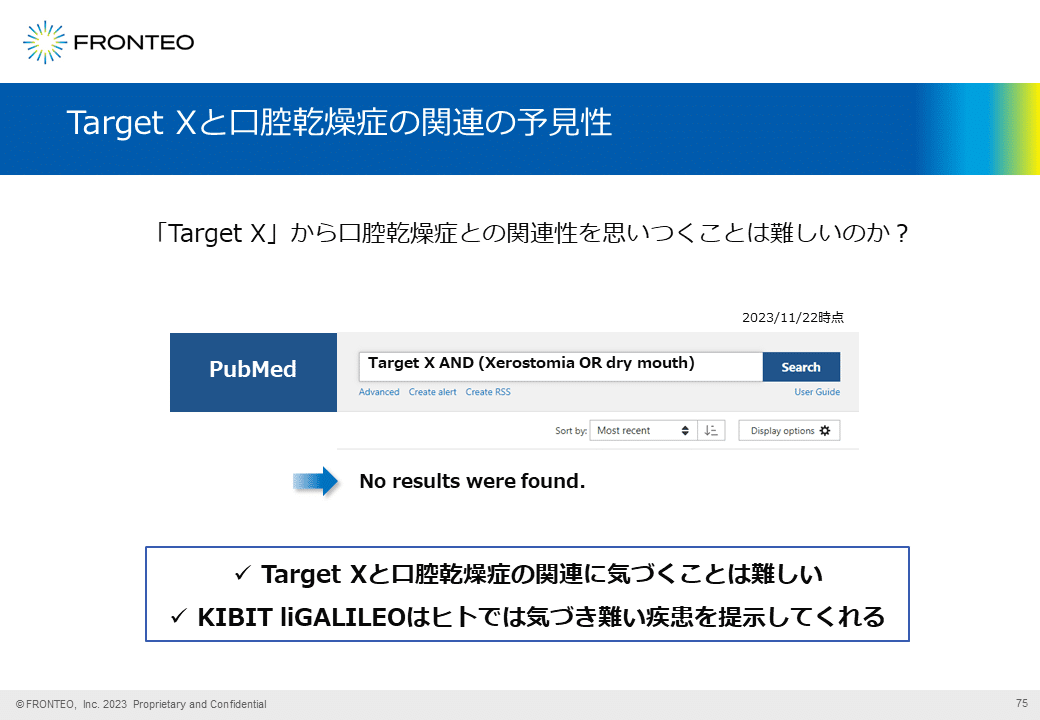
こうして見出されたTarget Xと口腔乾燥症の関連は、PubMedで検索すれば簡単に見つけられるのではないかという疑問が浮かぶかもしれません。Target Xと口腔乾燥症のand検索では、今回紹介した報告は検索結果に出てきませんでした。
このことから、FRONTEOの技術は、人では気づき難い疾患を提示できると言えます。
まとめ
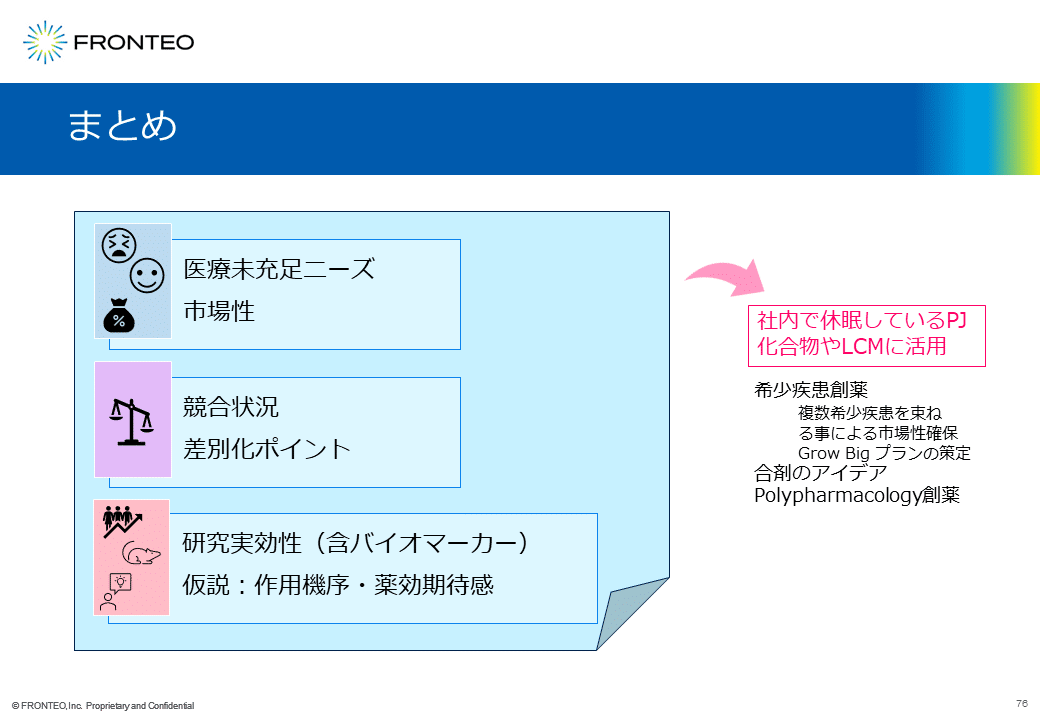
事例のような案件をFRONTEOへご依頼いただきましたら、市場性や医療ニーズ、差別化ポイントなどの簡易調査を行った上で、競合状況や研究の実効性、作用機序などの仮説まで作成・策定してご提供します。
こうした情報を、製薬会社様の社内で休眠しているプロジェクト化合物や、既存薬のライフサイクルマネジメントに活用いただければ幸いです。











